2023-2024 н.р.
ХІМІЯ - 8 клас
https://meet.google.com/kyf-hwgs-pzp - посилання на онлайн уроки (за розкладом)
10.05.2024 - 10.05.2024
Задача 1
П’ятачок на день народження друга вирішив надути повітряні кульки. Допоможіть йому обчисліть об’єм Гелію, кількістю речовини 3,5 моль.
Задача 2
Вчителька за урок витрачає 15 г крейди. Обчисліть кількість речовини та кількість молекул CaCO3.
Задача 3
Для приготування вечері Попелюшка використовує 1,5 моль NaCl. Обчисліть масу та кількість молекул солі.
Задача 4
Водяний в своєму ставку має 3000·1023 молекул води. Обчисліть масу та об’єм води в ставку.
Задача 5
Фея квітів має 150·1023 молекул чарівного пилу. Обчисліть кількість речовини та об’єм чарівного пилу.
Задача 6
Для приготування варення Карлсону потрібно 515 грам цукру. Обчисліть кількість речовини та кількість молекул цукру С12Н22О11.
Задача 7
Допоможіть Мауглі порахувати, яку кількість речовини та масу кисню виробляють дерева в джунглях, якщо відомо, що загальний об’єм O2 складає 5600 літрів.
Задача 8
Для боротьби з Десиптиконами людству вкрай необхідні кислоти HNO3 та H2SO4 масою 900 г та 750 г відповідно. Обчисліть к кількість речовини кислот.
( та об’єм, якщо r= 1,51 та r=1,84 вiдповiдно)
Задача 9
Дракон у своєму сховищі має 12000 · 1023 атомів золота та 9000 · 1023 атомів срібла. Обчисліть загальну масу його скарбів.
Задача 10
Для оборотного зілля Гаррі Потерру потрібно взяти 7 моль сірководню H2S. Допоможіть обчисліть, які необхідні об’єм та маса газу?
Д.З. Опрацюйте матеріал підручника п. 18-21, відеоматеріали, матеріали сайту (попередні відео та матеріали) . Виконані 10 задач = самостійній роботі з теми"Кількість речовини.
1 моль будь-якого газу за н. у. займає об’єм 22,4 л. Цей об’єм називають молярним об’ємом. Молярний об’єм чисельно дорівнює об’єму 1 моль речовини і позначається Vm («ве-ем»):
Vm = 22,4 л/моль, м3/моль.
Оскільки число молекул однакове, вага рівних об’ємів газів пропорційна молекулярним масам узятих речовин.
Молярний об’єм газу (Vm) визначається за відношенням об’єму (V) порції даного газу до кількості речовини (n) в цій порції: Vm = V / υ, де V – об’єм газу за н. у., (л, м3); ν – кількість речовини газу, (моль).
Отже, молярний об’єм газу вимірюється в літрах на моль (л/моль) або кубічних метрах на моль (м3/моль).
Визначення молярного об’єму газу за кількістю речовини і об’ємом
Приклад 22. Обчисліть молярний об’єм газу, 3 моль якого займають об’єм 67,2 л.
Дано: υ(газу) = 3 моль | Vm = V/ν; | Розв’язання: Обчислюємо молярний об’єм газу: |
Vm(газу) – ? |
Відповідь: Vm(газу) = 22,4 л/моль.
Молярний об’єм газу можна обчислити також, знаючи молярну масу газу та його густину ρ, тобто масу 1 л даного газу за нормальних умов.
Визначення молярного об’єму газу за густиною
Приклад 23. Обчисліть молярний об’єм амоніаку (NH3), маса 1 л якого за нормальних умов важить 0,76 г.
Дано: ρ(NH3) = 0,76 г/л | M(NH3) = 17 г/моль | Розв’язання: Обчислюємо молярний об’єм амоніаку: |
Vm(NH3) – ? |
Відповідь: Vm(NH3) = 22,4 л/моль.
Знаючи молярний об’єм газів, можна визначити: а) об’єм газу за відомою кількістю речовини; б) кількість речовини газу за відомим об’ємом; в) масу 1 літра газу, виміряного за нормальних умов, за відомою молярною масою; г) об’єм газу за відомою густиною та масою:
V = υ • Vm | υ = V / Vm | m = M / 22,4 | V = m / ρ |
Визначення об’єму газів
а) за кількістю речовини газу
Приклад 24. Обчисліть об’єм кисню кількістю речовини 2 моль.
Дано: n(O2) = 2 моль | V = υ • Vm | Розв’язання: Обчислюємо об’єм кисню кількістю речовини 2 моль: |
V(O2) – ? |
Відповідь: V(O2) = 44,8 л.
++++
Відносна густина газів – це відношення молярних мас двох газів, що займають однакові об’єми.
1. 2. 3.
|
|
|
| Якщо
|
Фізичний зміст відносної густини газів показує у скільки разів один газ важчий або легший за інший. З формул 2 і 3 можна визначити молярну і відносну молекулярну маси.
![]() або
або ![]()
Відносну густину газів обчислюють за будь-яким газом. Найчастіше визначають за воднем, киснем, повітрям.
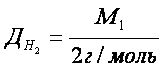
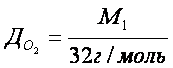
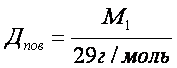
Д.З. Опрацюйте матеріал підручника п. 20-21, відеоматеріали, матеріали сайту.
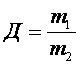
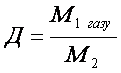
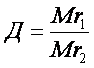
Немає коментарів:
Дописати коментар