КУРС "Біохімічні основи життя" - 10 клас
08. 04. 2022-15.04.2022
Тема: Екзони, інтрони. Поняття про сплансинг.
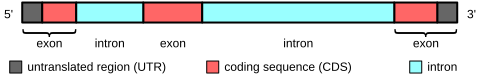
Екзон — ділянка ДНК в межах гену, яка переводиться у зрілу молекулу матричної РНК (мРНК) в процесах транскрипції і сплайсингу. Екзони більшості генів еукаріотів і деяких генів прокаріотів розділені сегментами некодуючої ДНК (інтронами), які видаляються під час сплайсингу.[1]
Екзон несе кодуючу послідовність до білка або його частини. Екзони розділені некодуючими послідовностями (інтронами). В еукаріотах більшість генів мають у своєму складі певну кількість екзонів.
Термін «екзон» ввів 1978 року американський біохімік Волтер Гілберт
Інтро́н — ділянка ДНК, яка є частиною гену, але на відміну від екзонів, не містить інформації про послідовність амінокислот білка.
Послідовність нуклеотидів, що відповідає інтрону, видаляється з транскрибованої з нього РНК в процесі сплайсингу до того, як відбудеться трансляція (зчитування білка). Інтрони характерні для всіх типів еукаріотичної РНК, але також знайдені в невеликій кількості в рибосомальній РНК (рРНК) і транспортній РНК (тРНК) прокаріотів. Число і довжина інтронів дуже різні в різних видах і серед різних генів одного організму. Наприклад, геном риби фугу (Takifugu rubripes) містить мало інтронов порівняно з іншими хребетними тваринами. З другого боку, гени ссавців і квіткових рослин часто містять численні інтрони, які можуть бути значно довше екзонів.
Хоча інтрони і не несуть інформації про послідовність амінокислот у білку, вони іноді дозволяють альтернативний сплайсинг гену, таким чином, що розділені інтроном ділянки можуть комбінуватися у різній послідовності, виробляючи різні варіанти білка з одного гену. Контроль сплайсингу мРНК і, в результаті, вибір кінцевого продукту, виконується широкою різноманітністю сигнальних молекул. Інтрони також іноді містять «застарілий код» секції гену, що ймовірно колись був частиною білка, але потім перестав використовуватися.
Загалом вважається, що послідовність інтронів є ділянкою ДНК без певної функції. Проте зараз це піддається сумніву: відомо, що інтрони містять декілька коротких послідовностей, які важливі для ефективного сплайсингу. Точний механізм дії цих інтронних енхансерів ще недостатньо відомий, але вважається, що вони служать обов'язковими ділянками ефективного синтезу білків, що стабілізують сплайсосому. Також можливо, що вторинна структура РНК, сформована з використанням послідовності інтронів, також має ефект на сплайсинг, інтронна послідовність при одному альтернативному сплайсингу стає екзонною при іншому. Послідовності «застарілого коду», з другого боку, в більшості випадків дійсно є «еволюційними артефактами».
Перший опис інтрону було зроблено в 1977 році Філіпом Шарпом і Річардом Робертсоном незалежно один від одного, за що вони були нагороджені Нобелівською премією з фізіології і медицини в 1993 року. Термін «інтрон» ввів американський біохімік Волтер Гілберт (англ. Walter Gilbert) в 1978 році.
Деякі інтрони, наприклад інтрони групи I і II, фактично є рибозимами, які здатні до каталізу свойого власного сплайсингу із первинної копії РНК. За це відкриття Чех Томас отримав Нобелівську премію з хімії, яку він розділив у 1989 році з Сіднеєм Алтманом. Крім того, інтрони можуть брати участь в експресії генів.
Сплайсинг — процес «вирізання» ново-синтезованої матричної РНК (мРНК) під час процесингу РНК. При сплайсингу з попередника мРНК (пре-мРНК) вилучаються інтрони, а екзони з'єднуються разом. Через те, що в геномах прокаріотів інтрони дуже рідкі (знайдені тільки в генах тРНК і рРНК), сплайсинг зазвичай характерний для еукаріотів. В результаті сплайсингу пре-мРНК перетворюється на зрілу мРНК, яка, якщо кодує білок, слідує на наступні кроки біосинтезу білків — транспортується з ядра до цитоплазми і транслюється у білок. Процес сплайсингу включає серії біохімічних реакції, які каталізуються сплайсосомою, комплексом малих ядерних рибонуклеопротеїнів (мяРНП). У багатьох випадках, сплайсинг призводить до утворення кількох унікальних типів білків, залежно від того, які інтрони вилучаються і які екзони з'єднуються — це явище називається альтернативним сплайсингом.
11. 03. 2022
Тема: Роль мітохондрій в енергетичному обміні клітин
Ще в далекому XIX столітті з інтересом вивчаючи за допомогою перших не досконалих ще тоді мікроскопів, будову живої клітини, біологи помітили в ній якісь довгасті зигзагоподібні об’єкти, які отримали назву «мітохондрії». Сам термін «мітохондрія» складений з двох грецьких слів: «мітос» – нитка і «хондрос» – зернятко, крупинка.
Мітохондрії являють собою двомембранний органоїд еукаріотичної клітини, основне завдання якого – окислення органічних сполук, синтез молекул АТФ, з подальшим застосуванням енергії, утвореної після їх розпаду. Тобто по суті мітохондрії це енергетична база клітин, говорячи образною мовою, саме мітохондрії є свого роду станціями, які виробляють необхідну для клітин енергію.
Кількість мітохондрій в клітинах може змінюватися від декількох штук, до тисяч одиниць. І більше їх природно саме в тих клітинах, де інтенсивно йдуть процеси синтезу молекул АТФ.
Самі мітохондрії також мають різну форму і розміри, серед них зустрічаються округлі, витягнуті, спіральні і чашоподібні представники. Найчастіше їх форма округла і витягнута, з діаметром від одного мікрометра і до 10 мікрометрів довжини.
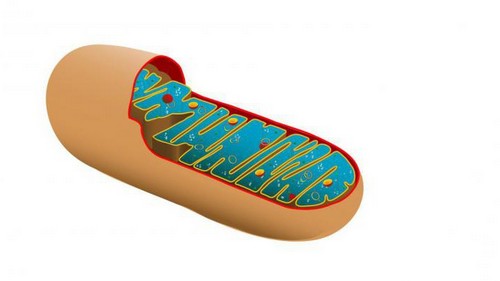
Приблизно так виглядає мітохондрія.
Також мітохондрії можуть, як переміщатися по клітині (роблять вони це завдяки току цитоплазми), так і нерухомо залишатися на місці. Переміщаються вони завжди в ті місця, де найбільш потрібно вироблення енергії.
Походження
Ще на початку минулого ХХ століття була сформована так звана гіпотеза сімбіогенезу, згідно з якою мітохондрії походять від аеробних бактерій, що потрапили в клітину прокаріотів. Бактерії ці стали постачати клітину молекулами АТФ натомість отримуючи необхідні їм поживні речовини. І в процесі еволюції вони поступово втратили свою автономність, передавши частину своєї генетичної інформації в ядро клітини, перетворившись в клітинну органелу.
Будова
Мітохондрії складаються з:
- двох мембран, одна з них внутрішня, інша зовнішня,
- міжмембранного простору,
- матриксу – внутрішнього вмісту мітохондрії,
- кристу – це частина мембрани, яка виросла в матриксі,
- білок синтезуючої системи: ДНК, рибосом, РНК,
- інших білків і їх комплексів, серед яких велике число всіляких ферментів,
- інших молекул.
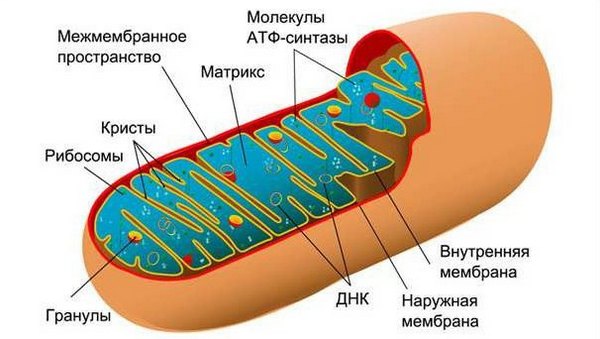
Так виглядає будова мітохондрії.
Зовнішня і внутрішня мембрани мітохондрії мають різні функції, і з цієї причини різниться їх склад. Зовнішня мембрана своєю будовою схожа з мембраною плазмовою, яка оточує саму клітину і виконує в основному захисну бар’єрну роль. Проте, дрібні молекули можуть проникати через неї, а ось проникнення молекул побільше вже вибіркове.
На внутрішній мембрані мітохондрії, в тому числі на її виростах – кристах, розташовуються ферменти, утворюючи мультиферментативні системи. За хімічним складом тут переважають білки. Кількість крист залежить від інтенсивності синтезуючих процесів, наприклад, в мітохондріях клітин м’язів їх дуже багато.
У мітохондрій, як втім, і у хлоропластів, є своя білоксинтезуюча система – ДНК, РНК і рибосоми. Генетичний апарат має вигляд кільцевої молекули – нуклеотиду, точнісінько як у бактерій. Частину необхідних білків мітохондрії синтезують самі, а частину отримують ззовні, з цитоплазми, оскільки ці білки кодуються ядерними генами.
Функції
Як ми вже написали вище, основна функція мітохондрій – постачання клітини енергією, яка шляхом численних ферментативних реакцій витягується з органічних сполук. Деякі подібні реакції йдуть за участю кисню, а після інших виділяється вуглекислий газ. І реакції ці відбуваються, як всередині самої мітохондрії, тобто в її матриксі, так і на кристах.
Якщо сказати інакше, то роль мітохондрії в клітині полягає в активній участі в «клітинному диханні», до якого відноситься безліч хімічних реакцій окислення органічних речовин, переносів протонів водню з подальшим виділенням енергії, тощо.
Ферменти
Ферменти транслокази внутрішньої мембрани мітохондрій здійснюють транспортування АДФ в АТФ. На голівках, що складаються з ферментів АТФази йде синтез АТФ. АТФаза забезпечує сполучення фосфорилювання АДФ з реакціями дихального ланцюга. У матриксі знаходиться велика частина ферментів циклу Кребса і окислення жирних кислот
11. 02. 2022
Тема: Поняття про біоенергетику АТФ
Що таке АТФ?
Безперечно, найважливішою молекулою в нашому організмі з точки зору виробництва енергії являється АТФ (аденозинтрифосфат: аденіловий нуклеотид, що містить три залишки фосфорної кислоти і утворюється в мітохондріях).
Насправді, кожна клітина нашого організму зберігає і використовує енергію для біохімічних реакцій за допомогою АТФ, таким чином, АТФ може вважатися універсальною валютою біологічної енергії. Усі живі істоти потребують безперервного енергопостачання для підтримки синтезу білку і ДНК, метаболізму і транспорту різних іонів і молекул, підтримки життєдіяльності організму. М'язові волокна в ході силових тренувань також вимагають легкодоступної енергії. Як уже згадувалося, енергію для усіх цих процесів поставляє АТФ. Проте для того, щоб сформувати АТФ, нашим клітинам потрібно сировину. Люди отримують цю сировину через калорії за допомогою окислення споживаної їжі. Для отримання енергії, ця їжа спочатку має бути перероблена в легко використовувану молекулу - АТФ.
Перед використанням молекула АТФ повинна пройти через декілька фаз.
Спочатку за допомогою спеціального коензиму відділяється один з трьох фосфатів (кожен з яких містить десять калорій енергії), завдяки чому вивільняється велика кількість енергії і формується продукт реакції аденозиндифосфат (АДФ). Якщо потрібно більше енергії, то відділяється наступна фосфатна група, формуючи аденозинмонофосфат (АМФ).
АТФ + H2O ---> АДФ + H3PO4 + енергія
АТФ + H2O --> АМФ + H4P2O7 + енергія
Коли швидке виробництво енергії не потрібно, відбувається зворотна реакція - за допомогою АДФ, фосфагену і глікогену фосфатна група знову приєднується до молекули, завдяки чому формується АТФ. Цей процес включає перенесення вільних фосфатів до інших речовин, що містяться в м'язах, до яких відносяться глюкоза і креатин. При цьому із запасів глікогену береться і розщеплюється глюкоза.
Отримана з цієї глюкози енергія допомагає знову перетворювати глюкозу в її первинну форму, після чого вільні фосфати знову можуть бути приєднані до АДФ для формування нового АТФ. Після завершення циклу знову створений АТФ готовий до наступного використання.
По суті АТФ працює, як молекулярна батарея, зберігаючи енергію, коли вона не потрібна, і вивільняючи у разі потреби. Дійсно, АТФ схожий на батарею, що повністю перезаряджається.
Структура АТФ
Молекула АТФ складається з трьох компонентів:
Рибоза (той же самий п'ятивуглецевий цукор, що формує основу ДНК)
Аденин (сполучені атоми вуглецю і азоту)
Трифосфат
Молекула рибози розташовується в центрі молекули АТФ, край якої служить базою для аденозину.
Ланцюжок з трьох фосфатів розташовується з іншого боку молекули рибози. АТФ насичує довгі, тонкі волокна, що містять білок міозин, який формує основу наших м'язових клітин.
Збереження АТФ
У організмі середньої дорослої людини щодня використовується близько 200-300 молі АТФ (моль - це хімічний термін, що означає кількість речовини в системі, в якій міститься стільки елементарних часток, скільки атомів вуглецю міститься в 0,012 кг ізотопу вуглецю-12). Загальна кількість АТФ в організмі в кожен окремо взятий момент складає 0,1 молі. Це означає, що АТФ повинен повторно використовуватися 2000-3000 разів впродовж дня. АТФ не може бути збережений, тому рівень його синтезу майже відповідає рівню споживання.
Системи АТФ
Зважаючи на важливість АТФ з енергетичної точки зору, а також із-за його широкого використання у організму є різні способи виробництва АТФ. Це три різні біохімічні системи.
Розглянемо їх по порядку:
Фосфагенна система
Система глікогену і молочної кислоти
Аеробне дихання
Фосфагенна система
Коли м'яз чекає короткий, але інтенсивний період активності (близько 8-10 секунд), використовується фосфагенна система - АТФ з'єднується з креатинфосфатом. Фосфагенна система забезпечує постійну циркуляцію невеликої кількості АТФ в наших м'язових клітинах.
М'язові клітини також містять високоенергетичний фосфат - фосфат креатину, який використовується для відновлення рівня АТФ після короткочасної, високо інтенсивної активності. Ензим креатинкіназа віднімає фосфатну групу у креатину фосфату і швидко передає її АДФ для формування АТФ. Отже, м'язова клітина перетворює АТФ на АДФ, а фосфаген швидко відновлює АДФ до АТФ. Рівень креатину фосфату починає знижуватися вже через 10 секунд високо інтенсивної активності, і рівень енергії падає. Прикладом роботи фосфагенної системи є, наприклад, спринт на 100 метрів.
Система глікогену і молочної кислоти
Система глікогену і молочної кислоти забезпечує організм енергією в повільнішому темпі, ніж фосфагенна система, хоча і працює відносно швидко і надає досить АТФ приблизно для 90 секунд високо інтенсивної активності. У цій системі молочна кислота утворюється з глюкози в м'язових клітинах в результаті анаеробного метаболізму.
Враховуючи той факт, що в анаеробному стані організм не використовує кисень, ця система дає короткочасну енергію без активації кардіо-респіраторної системи точно так, як і аеробна система, але із заощадженням часу. Більше того, коли в анаеробному режимі м'язи працюють швидко, могутньо скорочуються, вони перекривають вступ кисню, оскільки судини виявляються стислими.
Цю систему ще іноді називають анаеробним диханням, і хорошим прикладом в даному випадку послужить 400-метровий спринт.
Аеробне дихання
Якщо фізична активність триває більше двох хвилин, в роботу включається аеробна система, і м'язи отримують АТФ спочатку з вуглеводів, потім з жирів і нарешті з амінокислот (білків). Білок використовується для отримання енергії в основному в умовах голоду (дієти в деяких випадках).
При аеробному диханні виробництво АТФ проходить найповільніше, але енергії виходить досить, щоб підтримувати фізичну активність упродовж декількох годин. Це відбувається тому, що при аеробному диханні глюкоза розпадається на діоксид вуглецю і воду, не випробовуючи протидії з боку молочної кислоти в системі глікогену і молочної кислоти. Глікоген (накопичувана форма глюкози) при аеробному диханні поставляється з трьох джерел:
Всмоктування глюкози з їжі в шлунково-кишковому тракті, яка через систему кровообігу потрапляє в м'язи.
Залишки глюкози в м'язах
Розщеплювання глікогену печінки до глюкози, яка через систему кровообігу потрапляє в м'язи.
Висновок
Якщо ви коли-небудь замислювалися над тим, звідки у нас береться енергія для виконання різноманітних видів активності за різних умов, то відповіддю буде - в основному за рахунок АТФ. Ця складна молекула надає допомогу в перетворенні різних харчових компонентів в легко використовувану енергію.
Без АТФ наш організм просто не зміг би функціонувати. Таким чином, роль АТФ у виробництві енергії багатогранна, але в той же час проста.
04. 02. 2022
Тема: Прояв І і ІІ законів термодинаміки в живій природі
Термодинаміка – наука про перетворення енергії. Суть термодинамічного підходу – у розгляді лише початкового та кінцевого стану тіл, що взаємодіють, не беручи до уваги шлях, по якому протікає процес і час перетворення. Термінологія, що використовується в термодинаміці. Система – будь-яка сукупність тіл, відділена від зовнішнього середовища поверхнею розділу (реальною або уявною), всередині якої можливий масо- та теплообмін. Ізольованою системою, називається система, що не обмінюється з навколишнім середовищем ні масою, ні енергією (Δm = 0, ΔU = 0). Закрита система — обмінюється з навколишнім середовищем тільки енергією (Δm = 0, ΔU ≠ 0). Відкрита система - обмінюється з навколишнім середовищем і масою, і енергією (Δm ≠ 0, ΔU ≠ 0). З погляду термодинаміки живий організм відноситься до відкритих систем. Стан системи – це сукупність її фізичних і хімічних властивостей; він характеризується термодинамічними параметрами. Основні з них: температура T, тиск Р, об'єм системи V, загальна маса системи m, маси хімічних речовин (компонент) mк, з яких складається система, або концентрація цих речовин Ск. 2. Перший закон термодинаміки. Ентальпія. Екзотермічні і ендотермічні процеси Якщо відсутній теплообмін системи із зовнішнім середовищем, то величина внутрішньої енергії залишається постійною. По суті — це закон збереження енергії – перший закон термодинаміки. Іншими словами, енергія не може ні створюватися, ні зникати, вона може тільки переходити з однієї форми в іншу. Це фундаментальний закон природи. Теплота, підведена до системи, витрачається на збільшення внутрішньої енергії ΔU і здійснення роботи проти зовнішніх сил А: Q = ΔU+ А – це математичний вираз першого закону термодинаміки.
Закон Гесса – основний закон термохімії. Термохімічні розрахунки для оцінки калорійності продуктів Наслідком першого закону термодинаміки є закон Гесса (основний закон термохімії): Тепловий ефект хімічних реакцій, що протікають при постійному об'ємі або тиску, не залежить від числа проміжних стадій і визначається тільки початковим і кінцевим станом системи. Закон Гесса дозволяє обчислити теплові ефекти таких реакцій, які або взагалі не протікають в умовах досліду, або для них неможливе визначення теплового ефекту (у випадку нестабільних сполук). Із закону Гесса витікає: тепловий ефект реакції (ентальпія) дорівнює алгебраїчній сумі ентальпій утворення продуктів реакції за винятком алгебраїчної суми ентальпій утворення вихідних речовин враховуючи стехіометричні коефіцієнти (перший наслідок). З теплотами згоряння (мова йде про реакції окислювання киснем) зв'язаний другий наслідок із закону Гесса: Тепловий ефект реакції дорівнює різниці сум стандартної ентальпії згоряння вихідних речовин і стандартних ентальпій згоряння продуктів реакції, взятих у відповідності зі стехіометричними коефіцієнтами. Стосовно до живих систем перший закон термодинаміки можна сформулювати так: всі види робіт в організмі відбуваються за рахунок еквівалентної кількості енергії, що виділяється при окисненні поживних речовин. Енергетичний баланс організму вивчається методами прямої і непрямої калориметрії. У першому випадку людину поміщають в ізольовану камеру, в якій визначають кількість теплоти, що випромінюється живим організмом при різних процесах нормальної фізіологічної діяльності. Непряма калориметрія заснована на розрахункових методах з використанням дихальних коефіцієнтів і калоричного еквіваленту кисню.
05. 11. 2021
Тема: Клітина. Буферні властивості клітини.
Клітина - це структурна одиниця живих організмів, що є певним чином диференційованою ділянкою цитоплазми, оточеною клітинною мембраною. Функціонально клітина є основною одиницею життєдіяльності організмів.
Хоча клітини (рослин, тварин і грибів) мають різну будову і виконують різні функції, вони мають багато спільних морфологічних особливостей (сформоване ядро, подібний набір органел) і подібних функціональних властивостей (біосинтез білків, використання і перетворення енергії, процеси розмноження).
Внутрішній вміст клітини (протоплазма) ділиться на цитоплазму і ядро. Цитоплазма є основною за об'ємом частиною клітини. За фізичними властивостями це напіврідка маса колоїдної структури, в якій містяться органели клітини мембранної (ендоплазматична сітка, мітохондрії, пластиди, комплекс Гольджі, лізосоми) і не-мембранної (рибосоми, центріолі клітинного центру) будови. Агрегатний стан цитоплазми може бути різним: рідким - золь і в'язким - гель. За хімічним складом цитоплазма досить складна.
Під оптичним мікроскопом у цитоплазмі не вдається розгледіти жодних структур, і вона здається однорідною. За допомогою електронного мікроскопа було встановлено, що в цитоплазмі всіх клітин тваринного і рослинного походження є складна система мембран, які часто розміщуються паралельно одна одній. Ця система мембран дістала назву ендоплазматичної сітки.
Мембрани завтовшки 6-8 нм мають ліпідно-білкову природу і за структурою подібні до зовнішньої мембрани клітини. Вони обмежують дуже розгалужену взаємозв'язану систему канальців, щілин і міхурців, яка сполучає різні ділянки клітини. Діаметр порожнини канальців - 25-30 нм. Мембрани ендоплазматичної сітки безпосередньо зв'язані з мембранами комплексу Гольджі. З мембран ендоплазматичної сітки утворюється оболонка ядра після поділу клітини. Зовнішня оболонка ядра є продовженням мембрани ендоплазматичної сітки і навколо-ядерний простір сполучений з простором ендоплазматичної сітки.
Пластиди - органели, специфічні для рослинних клітин, а в клітинах тваринних організмів, бактерій, синьозелених водоростей і грибів їх немає. У клітинах вищих рослин міститься від 10 до 200 пластид розміром 3-10 мкм, більшість із них має форму двоопуклої лінзи (трапляються у формі паличок, пластинок, лусок і зерен).
Залежно від характеру пігменту розрізняють:
- хлоропласти (гр. chioros - зелений) - зеленого кольору,
- хромопласти - жовтого, оранжевого і червоного кольорів,
- лейкопласти - безбарвні пластиди.
У процесі розвитку рослин пластиди одного типу можуть перетворюватися на пластиди іншого типу. Це явище поширене в природі й особливо помітне під час достигання плодів, коли змінюється їхнє забарвлення. У більшості водоростей пластиди представлені хроматофорами (у клітині він зазвичай один, значних розмірів і має форму сітки, чаші, спіральної стрічки або зірчастої пластинки).
Б у ф е р н і р о з ч и н и
Розчини, що підтримують певне значення рН, окисновідновного потенціалу або інших характеристик середовища називають буферними розчинами. Кислотно-основні буферні розчини містять суміш слабкої кислоти й її солі, або слабкої основи й її солі та зберігають сталу концентрацію іонів водню при додаванні до них певної кількості кислоти, лугу або при розведенні. Велике значення в організмі людини мають гідрокарбонатна і фосфатна буферні системи. Гідрокарбонатна буферна система NaНСО3/Н2СО3 присутня у крові і позаклітинному середовищі. Приклади буферних розчинів, які застосовуються у біохімічних
Немає коментарів:
Дописати коментар